精准肿瘤学发展现状:从基因检测到靶向治疗
| 精准肿瘤学发展现状:从基因检测到靶向治疗 |
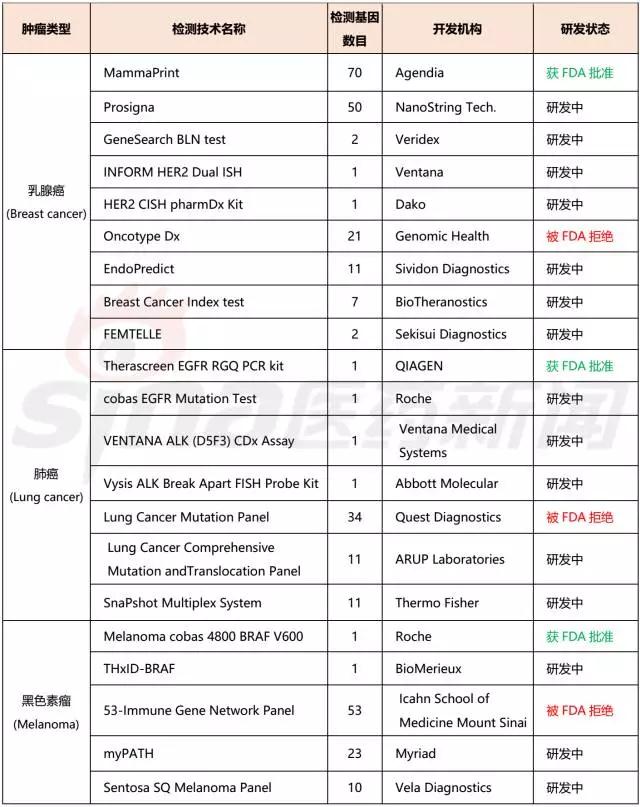
近年来,随着高通量测序及生物信息学分析技术的不断提高,精准医疗的理念逐渐受到关注。2015年1月20日,美国总统奥巴马在国情咨文中提出“精准医学计划”,希望精准医学可以引领一个新的医学时代。 精准医疗本质上是通过基因组、蛋白质组等组学技术和医学前沿技术,对于大样本人群与特定疾病类型进行生物标记物的分析与鉴定、验证与应用,从而精确寻找到疾病的原因和治疗的靶点,并对一种疾病不同状态和过程进行精确分类,最终实现对于疾病和特定患者进行个性化精准治疗的目的,提高疾病诊治与预防的效益。 目前,肿瘤的治疗成为精准医疗的主战场。研究人员已发现,许多分子病变是驱动癌症的诱因,这表明每种癌症都有自己的基因印记、肿瘤标记物以及不同的变异类型。虽然癌症主要是由日常生活中基因损伤积累所导致的,但可遗传性基因变异通常会增加患癌风险。当下,肿瘤的治疗已逐渐告别既往的经验性治疗模式向循证、精准方向迈进。 精准肿瘤学的目标是甄别具有共同生物学基础的患者群体,选择最有可能受益的药物或治疗方式,提高诊治效益。它包括精准预防、精准诊断、和精准治疗。本文以乳腺癌、肺癌和黑色素瘤为例,介绍精准诊断与精准治疗的发展现状,以及面临的一些问题。 基因检测 精准诊断不仅能帮助临床医生识别肿瘤的类型和阶段,还能揭示致癌的基因突变,这为精准治疗奠定了坚实的基础。精准诊断的目标包括优化临床结果,避免不必要的治疗,降低治疗副作用,以及避免耐药性的发生。 BRCA1/2基因的发现是精准诊断发展的里程碑事件。BRCA1/2是从一个乳腺癌家系中发现的,研究表明,该基因的突变与乳腺癌有着某种关联。目前,BRCA1/2和其它的乳腺癌易感基因的基因检测,成了肿瘤精准检测的经典范例,全球大约有100万人接受了BRCA1/2突变检测。BRCA1的突变类型大概有1800种,BRCA2的突变类型大概有2000种。在乳腺癌突变基因中,BRCA1/2发生变异的影响要超过tumor protein p53 (TP53)、phosphatase and tensin homolog (PTEN)、liver kinase B1 (LKB1)、cadherin1(CDH1)等基因发生变异的影响。 基因检测已被开发用于肿瘤的诊断、预测和预后等方面,其中一些已经得到食品和药物管理局的批准,而另一些仍在开发中。如表1所示。在乳腺癌基因检测方面,由Agendia公司开发的涉及70个检测基因的MammaPrint,目前已被FDA批准;在肺癌基因检测方面,由QIAGEN公司开发的涉及1个检测基因的Therascreen EGFR RGQ PCR kit,目前已被FDA批准;在黑色素瘤基因检测方面,由Roche公司开发的涉及1个检测基因的Melanoma cobas 4800 BRAF V600,目前已被FDA批准。此外,还有许多检测手段处于研发阶段。 表1 乳腺癌、肺癌和黑色素瘤的基因检测发展情况
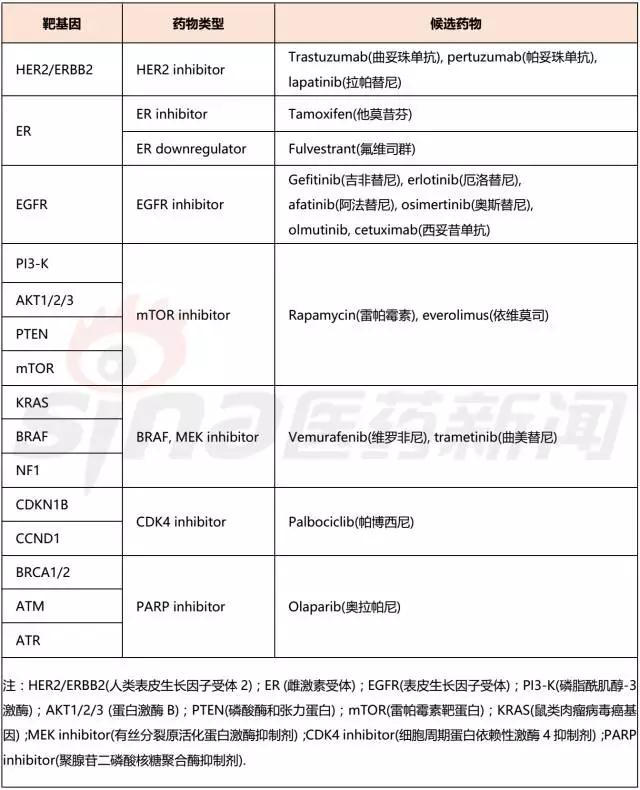
注:点击图片可查看清晰大图 靶向治疗 在考虑哪些患者进行靶向治疗以及有效治疗策略的监测时,肿瘤标志物十分关键。它们可以通过监测疾病进展和疗效,鉴别疾病阶段和亚型,以及预后来提高临床诊断的准确性。 在乳腺癌的靶向治疗上,最经典的靶标应该是雌性激素(estrogen receptor , ER)和人类表皮生长因子受体2(HER2),HER2能够与EGFR、HER3、HER4等酪氨酸激酶受体形成异二聚体,HER2的过表达能够诱导乳腺癌的发生。Tamoxifen(他莫昔芬),一种拮抗雌激素的前药,其在肝脏内的代谢中间产物与雌激素具有很强的结合力;Trastuzumab(曲妥珠单抗),一种单克隆抗体,能够HER2相结合,抑制其活性,适用于HER2过表达的乳腺癌患者。目前,乳腺癌其它的的一些靶向治疗药物如表2所示。 表2 乳腺癌的靶向治疗
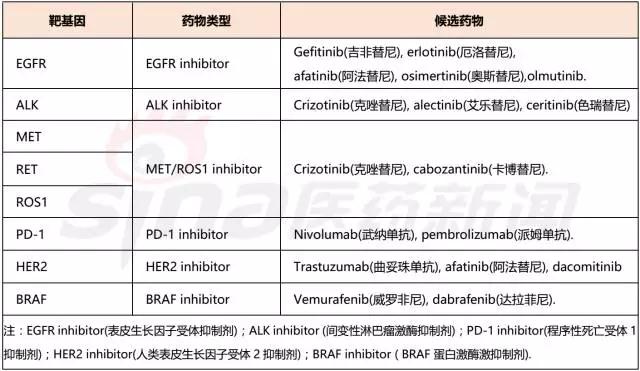
注:点击图片可查看清晰大图 在肺癌的靶向治疗上,靶向药物主要有EGFR inhibitor(表皮生长因子受体抑制剂)、ALK inhibitor (间变性淋巴瘤激酶抑制剂)、BRAF inhibitor (BRAF蛋白激酶激抑制剂)、以及免疫检查点抑制剂,如表3所示。 Gefitinib(吉非替尼),一种表皮生长因子受体抑制剂,因较好的治疗效果,较低的毒副反应,一上市就取代了传统的肺癌治疗药物,成为肺癌的一线治疗药物。但是,几乎所有使用EGFR抑制剂的患者都出现了耐药性,这是因为EGFR 发生了二次突变,比如T790M。因此,针对EGFR易突变的特性,出现了第二代表皮生长因子受体抑制剂,比如afatinib(阿法替尼)。第三代表皮生长因子受体抑制剂,osimertinib(奥斯替尼)和olmutinib也已经分别在美国、韩国上市,它们能够不可逆性地与EGFR T790M相结合。 Crizotinib(克唑替尼),一种ALK、MET和ROS1抑制剂。与传统的化疗药物相比,Crizotinib(克唑替尼)已经展示出对ALK阳性肺癌患者、ROS1重排的非小细胞肺癌患者的疗效、安全性等方面的优势。ALK的某些突变型,比如R1174L、L1196M和R1275Q,会对克唑替尼产生耐药性,这导致了下一代ALK抑制剂的问世,比如,Ceritinib(色瑞替尼)靶向L1196M;Alectinib(艾乐替尼)靶向R1174L、L1196M。 肿瘤细胞通过自身的PD-L1与T细胞的PD1相互作用,来逃避免疫系统的的“监管”,目前,Nivolumab(武纳单抗)和Pembrolizumab(派姆单抗)已被FDA批准用于非小细胞肺癌患者的二线治疗。 表3 肺癌的靶向治疗
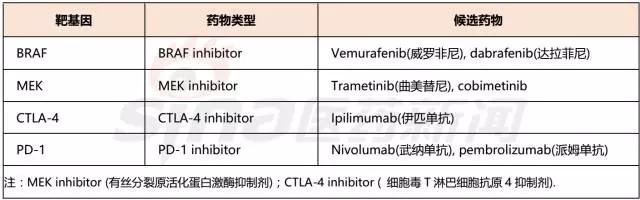
据统计,40%的黑色素瘤患者中,BRAF基因会发生突变。BRAF位于在丝裂原活化蛋白激酶(mitogen-activated protein kinases,MAPKs)信号通路(Ras-Raf-MEK-ERK)中。最常见的突变型是V600E 和V600K,二者分别占73%、19%。BRAF 抑制剂主要是Vemurafenib(威罗非尼)、dabrafenib(达拉菲尼),因为黑色素瘤极易产生耐药性,临床上采取BRAF 抑制剂和CTLA-4 抑制剂联合用药的策略。 黑色素瘤细胞会产生CTLA-4和PD1免疫受体蛋白,这些蛋白会抑制T细胞的免疫功能。CTLA-4抑制剂Ipilimumab(伊匹单抗)和PD-1抑制剂Nivolumab(武纳单抗)、Pembrolizumab(派姆单抗)已经获得FDA批准,二者联合用药用于黑色素瘤。 表4 黑色素瘤的靶向治疗
面临的障碍 目前,精准肿瘤学在临床上还面临着一些障碍。首要的是特定的分子靶向药物的短缺,一些靶向药物因毒副作用、高昂花费等因素面临着使用的困境。 在大规模基因组测序下,也只有肿瘤类型和大小等少量的临床数据是可用的。临床数据的准确性是有限的,并且常常缺少关键的临床信息,例如诊断时的肿瘤分期,肿瘤分级,组织类型,复发类型和存活时间等。 另一方面,据估计,每个癌症患者存在5-6个遗传突变位点,但对于不同个体和不同肿瘤存在着差异。基因突变的类型和数量的复杂性可能是精准肿瘤学研究的一大障碍。 此外,有广泛的证据表明癌细胞可以适应和逃避靶向药物,还可以通过突变的目标基因或通过激活代偿途径绕过药物的抑制作用。然而,这些理论中很少被充分表征或在临床中应用以抵抗耐药性。此外,微环境在药物敏感性中的作用仍是进一步探索的主题。 总之,精准肿瘤学的到来并不意味着循证医学的结束。相反,我们期待着精准肿瘤学能带来更好的临床试验的设计,完善的临床诊断和更精确的治疗。 |