100%有效预防艾滋!HIV药物市场生变
近期,艾滋病预防药物迎来重大突破,吉利德的lenacapavir在女性艾滋病暴露前预防(PrEP)3期临床试验中实现100%有效,这是全球首次艾滋病预防药物在3期临床中实现100%有效。
吉利德在HIV药物领域处于领先地位,其Biktarvy常年霸占抗HIV药物冠军宝座,2022年和2023年销售额都突破百亿美元,但Biktarvy需要每日口服给药,每年仅需给药两次的长效制剂lenacapavir,更加巩固了吉利德在HIV药物的地位。
除吉利德外,GSK和强生的HIV药物也占有很大市场份额,lenacapavir的成功,势必进一步重塑市场竞争格局。
半年一针,100%有效
Lenacapavir是一款首创长效人类免疫缺陷病毒(HIV)衣壳抑制剂,主要通过干扰病毒生命周期的多个重要步骤来抑制HIV-1复制,于2022年8月首次在欧洲获批上市,随后同年12月被FDA批准上市,是全球唯一一款获批上市的每年给药2次的HIV治疗药物。
Lenacapavir获FDA批准得到了2/3期CAPELLA试验数据的支持,该试验评估了lenacapavir联合优化的背景方案治疗具有大量治疗经验的多重耐药HIV-1患者。CAPELLA参与者之前接受过中位数为九种抗逆转录病毒药物的治疗。
在这个医疗需求明显未得到满足的患者群体中,83%(n=30/36)的受试者被随机分配接受Lenacapavir治疗,在第52周时达到了检测不到的病毒载量(<50拷贝/mL)。此外,这些参与者的CD4计数平均增加82个细胞/μL(图1)[1,2]。
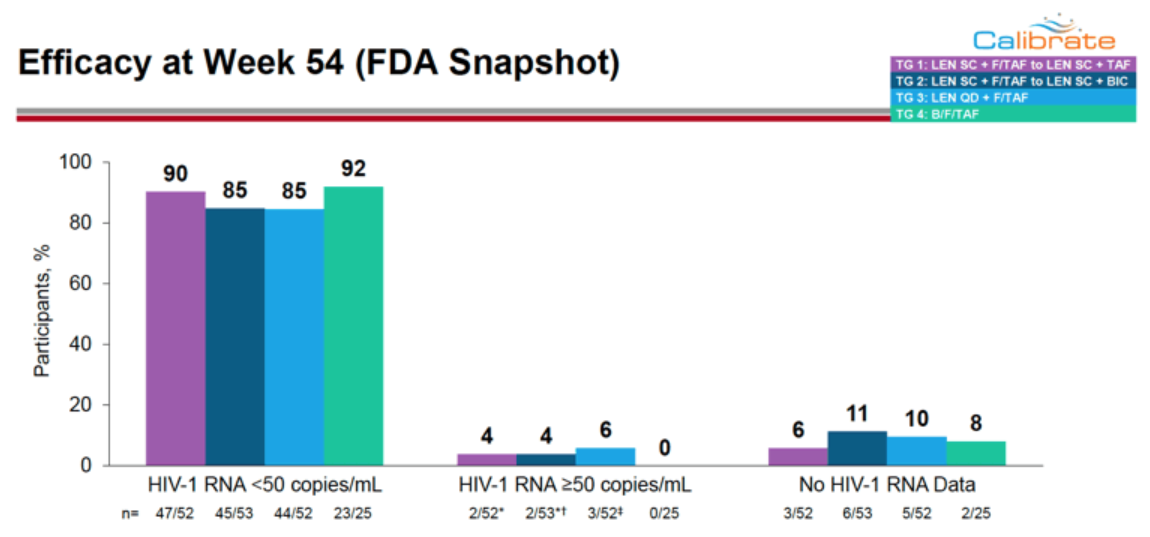
图1 CAPELLA试验结果
图片来源:参考文献2
Lenacapavir是一项突破性的创新药物,由于其治疗效力以及一系列给药频率和给药途径,有可能成为一种首选和多功能的基础长效药物。
Lenacapavir的另一项关键试验PURPOSE2将在2024年底/2025年初获得结果,该试验正在评估阿根廷、巴西、墨西哥、秘鲁、南非、泰国和美国的男男性行为者、跨性别男性、跨性别女性和与出生时被指定为男性的伴侣发生性关系的非二元性别个体的暴露前预防(PrEP)使用lenacapavir。
除此之外,Lenacapavir还开展了2期PURPOSE3(HPTN-102,NCT06101329)和PURPOSE4(HPTN-103,NCT06101342)试验,目前PURPOSE3正在招募美国HIV女性,重点是黑人女性和其他有色人种女性。
全球获批,三足鼎立
HIV是一种逆转录病毒,其逆转录过程就是在病毒逆转录酶的作用下,以病毒RNA为模板合成前病毒DNA的过程。
抗逆转录病毒疗法(ART)是目前治疗逆转录病毒(主要HIV)感染的主要疗法,可以阻止HIV进入人体细胞或阻断HIV在人体细胞内复制和/或将其遗传物质整合到人类DNA中所需的其中一种酶的活性。
ART药物的主要分为7大类:核苷类逆转录酶抑制剂(NRTI)、非核苷类逆转录酶抑制剂(NNRTI)、整合酶抑制剂(INSTI)、蛋白酶抑制剂(PI)、整合酶链转移抑制剂(INSTI)、融合抑制剂(FIs)、CCR5抑制剂和新型作用机制药物(如CD4吸附后抑制剂)。
全球范围抗HIV的主要研有吉利德、GSK、默克、强生、默沙东等多家跨国企业,其中吉利德、GSK、强生已成为HIV全球药物市场前三强,市场份额均在不断扩张(表1)[3]。
表1全球部分获批的抗HIV药物
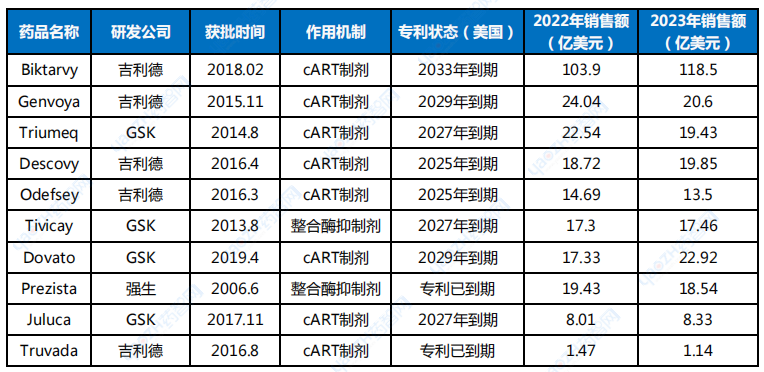
数据来源:公开资料整理
吉利德近年来不断推出创新重磅产品,凭借多款艾滋病口服药物如Biktarvy、Genvoya、Descovy、Odefsey等占据主导地位,据吉利德2023年财报显示,2023年吉利德全年营收269亿美元,HIV药物销售额181.75亿美元,其中Biktarvy销售额118.5亿美元,同比增长14%。
Biktarvy是现有的基于整合酶链转移抑制剂的最小的三联复方单片制剂,由bictegravir50mg、emtricitabine200mg和tenofoviralafenamide25mg组成,于2018年2月在美国获批上市,用于治疗HIV-1感染的儿科患者(体重≥25公斤)和成人患者。
除Biktarvy之外,吉利德的Genvoya、Descovy、Odefsey等多款HIV药物在全球范围内都比较抢手,其中2023年Genvoya销售额为20.6亿美元,Descovy销售19.85亿美元、Odefsey收入13.5亿美元,这几款药物撑起了吉利德的HIV市场的霸主地位。
GSK在艾滋病领域稳坐第二把交椅,1987年全球首个艾滋病药物齐多夫定便是由GSK开发上市,GSK又开发了Triumeq片(阿巴卡韦600mg、Dolutegravir50mg及拉米夫定300mg)、Combivir(拉米夫定/齐多夫定)、Trizivir(阿巴卡韦/拉米夫定/齐多夫定)、Epzicom/Kivexa(阿巴卡韦/拉米夫定)等一系列鸡尾酒疗法。
2015年12月,GSK旗下ViiV医药保健公司宣布将以约14.55亿美元打包收购BMS全部在研艾滋病药物,进一步扩充了其研发管线。
Triumeq于2014年8月在美国获批上市,上市第二年至2022年Triumeq销售额基本能保持前三位置,2022年的销售额为22.54亿美元,2023年被GSK另一款HIV药物Dovato反超,销售额为19.43亿美元,而Dovato的销售额涨至22.92亿美元。
目前,国内市场在售的HIV药物以进口药及国产仿制药为主,进口药由吉利德、GSK、强生、默沙东等几家企业掌控80%的市场份额,仿制药由超过40家国内企业布局,包括迪赛诺、齐鲁药业、倍特药业、安贝克生物和东北药业等。
除此之外,也有4款国产HIV创新药获批上市,分别是艾迪药业的艾邦德和复邦德,前沿生物的艾可宁和真实生物的阿兹夫定片。
艾邦德于2023年1月4日在国内获批上市,是首个国产三合一艾滋病新药,用于治疗成人HIV-1感染初治患者。
全球在研,潜力无限
弗若斯特沙利文报告显示,全球抗HIV药物市场规模2017年为325亿美元,预计2025年将达到479亿美元,2030年将达到575亿美元,2021年至2025年的复合年增长率为6.0%,2025年至2030年的复合年增长率为3.7%。
凭借在HIV领域多年的经验,吉利德进一步深耕HIV药物,正在开发bictegravirandlenacapavir每日口服一次组合疗法、Lenacapavir和广泛中和抗体(bNAb)组合疗法以及新型每周一次的整合酶链转移抑制剂GS-1720等[4]。
今年3月份,吉利德宣布了旨在比较整合酶链转移抑制剂bictegravir和同类首创衣壳抑制剂lenacapavir的每日一次组合疗法与当前治疗在复杂方案中病毒学抑制的HIV感染者的治疗的ARTISTRY-1(NCT05502341)的关键数据。
研究结果显示:所有三个治疗组在六个月时都具有强大的病毒学抑制,在整个研究过程中病毒载量始终较低。到第24周,低剂量lenacapavir组合疗法或稳定基线方案组的参与者均未出现病毒载量反弹(≥50拷贝/mL)。在较高剂量的lenacapavir组合疗法中,只有一名受试者的病毒载量高于阈值,后来在不改变方案的情况下被抑制(图2)[5]。
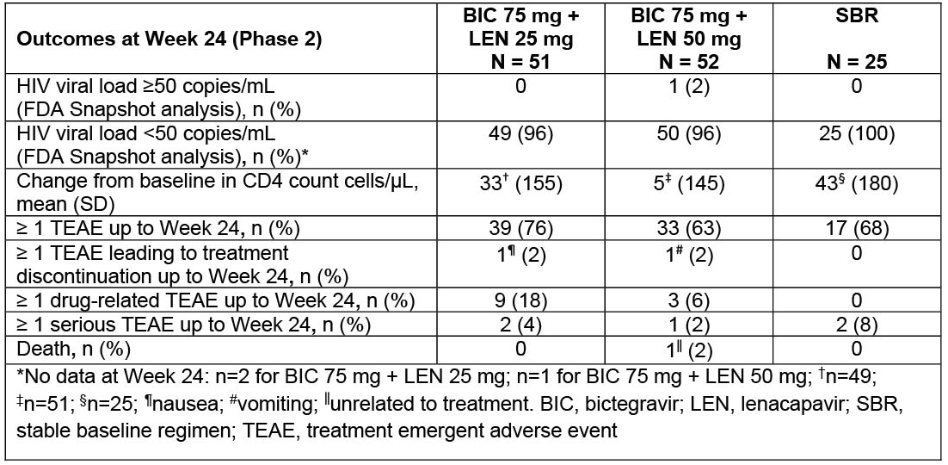
图2 ARTISTRY-1试验结果
图片来源:参考文献5
今年1月份,每年给药两次的lenacapavir+bNAb(teropavimab+zinlirvimab)组合疗法的一项1b期研究结果被发表在《柳叶刀HIV》上[6]。
研究结果显示:在六个月时,该长效组合疗法耐受性良好,安全性良好,8/10的参与者维持病毒学抑制(HIV病毒载量≤50拷贝/mL)。此外,高剂量zinlirvimab组的六名参与者在六个月时都保持了病毒学抑制,显示了这种研究性长效治疗方案的潜力,每年给药两次。
该长效组合疗法已进入2期研究(NCT05729568),将评估该方案在病毒学抑制的参与者中对多剂量研究方案进行纵向随访的安全性和有效性。
GS-1720是一种选择性整合酶链转移抑制剂,被评估为一种新型的、研究性的每周一次的抗逆转录病毒药物,与长效药物联合使用,旨在为HIV感染者提供新的长效选择。
GS-1720的一项正在未接受过治疗或病毒血症且停止抗逆转录病毒治疗至少12周的HIV感染者中进行1b期试验结果显示:与基线相比,GS-1720在剂量超过150mg的参与者中显示出潜在的抗病毒活性。
GS-1720耐受性良好,没有参与者出现任何严重的AE、3级或更高级别的TEAE或与研究药物相关的AE。在第11天,450mg和150mg队列未观察到治疗中出现的INSTI耐药性,其他剂量组的耐药性测试正在进行中。这些发现支持对GS-1720的持续临床评估,作为潜在的每周一次口服HIV治疗方案。
eOD-GT860mer最早由由InternationalAIDSVaccineInitiative,Inc.(国际艾滋病疫苗行动组织公司,IAVI)公司最早进行研发的一种自组纳米颗粒形式HIV疫苗工程蛋白(Env),是第一个进入使用基于结构的疫苗方法设计的临床试验的候选药物。
2022年12月,eOD-GT860mer的一项I期临床试验IAVIG001结果被发表在《Science》上,结果显示eOD-GT860mer具有良好的安全性,在36名接种者中,97%(35人)产生了广泛中和抗体。
IAVI还与生物技术公司Moderna在eOD-GT860mer基础上合作开发和测试了基于mRNA技术的HIV疫苗,并于2021年进行了非mRNA技术的1期临床试验,目前Moderna有mRNA-1644和mRNA-1574两条在研的HIV疫苗管线(图3)。

图3 Moderna的HIV管线
图片来源:Moderna官网
结语
艾滋病人群基数巨大,但目前尚无可以完全治愈艾滋病的药物,目前在市场上常用的抗HIV药物需要每天口服,在暴露前预防。
但是每日口服药物患者依从性不高,且容易忘记导致效果达不到预期,因此需要更长效、高效的抗HIV药物,lenacapavir此次在女性艾滋病暴露前预防3期临床试验中实现100%有效意义重大,有望进一步提升lenacapavir的市场份额,改变抗HIV药物市场。
参考文献
1.Sunlenca®(lenacapavir)ReceivesFDAApprovalasaFirst-in-Class,Twice-YearlyTreatmentOptionforPeopleLivingWithMulti-DrugResistantHIV
2.LenacapaviraspartofaCombinationRegimeninTreatment-NaïvePeoplewithHIV:Week54Results
3.博药:40余年艾滋病药物“进化史”,谁主沉浮?
4.Gilead’sInnovativeHIVTreatmentResearchPipelineAimstoAddressUnmetNeedsandAdvancePublicHealth
5.PhaseIIStudyofSwitchtoDailyBIC+LENinIndividualsonaMultitabletHIVTreatmentRegimen
6.JosephJEron,Safetyofteropavimabandzinlirvimabwithlenacapavironceevery6monthsforHIVtreatment:aphase1b,randomised,proof-of-conceptstudy,LancetHIV2024;11:e146–55




